类风湿小结是类风湿关节炎的一个特征性病理标志,它并非出现在所有患者中(发生率约20-30%),但一旦出现,对于疾病的诊断具有非常重要的价值。
(图片来源网络,侵删)
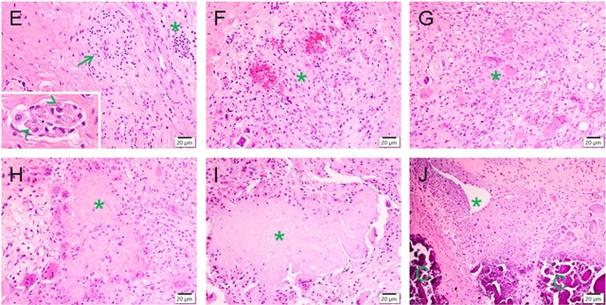
类风湿小结是一个发生在关节外组织的肉芽肿性病变,其核心病理特征是纤维素样坏死,周围有炎性细胞浸润,最外层被成纤维细胞和血管包绕,形成类似“洋葱皮”样的结构,它主要位于受压或摩擦的部位,如肘关节鹰嘴、手指伸肌腱、跟腱等,但也可能出现在内脏器官,如肺、心包和脾脏。
显微镜下的病理分层结构(从中心到外周)
典型的类风湿结节在显微镜下呈现出非常清晰的分层结构,就像一个靶心或洋葱头。
中心区:纤维素样坏死
- 成分:这是结节最核心、最具特征性的部分,它并非真正的“纤维”组织,而是一种无结构的、嗜伊红性(在染色中呈鲜红色)的坏死物质。
- 来源:这种坏死物质主要由以下成分混合而成:
- 纤维蛋白原:从血管中渗出并凝固。
- 免疫复合物:抗原(如自身抗体、变性IgG)与抗体(如类风湿因子RF)结合形成的沉淀物。
- 核碎片:坏死的中性粒细胞等细胞的细胞核碎片。
- 特点:这片坏死区是无细胞结构的,呈现一片均质的、深染的红色。
中间区:“栅栏状”或“袖套状”细胞浸润
- 位置:紧邻坏死区的外围。
- 细胞类型:主要由巨噬细胞和成纤维细胞构成,并呈栅栏状或袖套状整齐地排列在坏死区的边缘。
- 形态:这些细胞体积较大,胞质丰富,细胞核呈卵圆形,形态上类似于上皮样细胞,这种排列方式是肉芽肿性炎症的典型特征,类似于结核结节中的朗汉斯巨细胞排列。
外周区:慢性炎症细胞浸润
- 位置:最外层,与周围组织相接。
- 细胞类型:主要为淋巴细胞(以T细胞为主)和浆细胞,有时还能看到中性粒细胞和嗜酸性粒细胞的浸润。
- 特点:这一区域的炎症细胞分布相对疏松,不像中间区那样排列整齐,这些细胞反映了持续的免疫反应和炎症状态。
最外层:纤维组织包绕
- 结构:整个结节的外围被一层致密的纤维结缔组织(胶原纤维)包裹。
- 来源:由外周的成纤维细胞增生形成。
- 作用:这层纤维包囊起到了物理隔离作用,将坏死物质与周围正常组织分开,防止其进一步扩散。
免疫组化特点
免疫组化染色可以帮助我们更精确地识别结节中的各种成分,从而深化对病理机制的理解。
- CD68:在中间区的巨噬细胞/上皮样细胞中呈阳性,证实了它们的组织来源。
- CD3, CD20:分别标记T细胞和B细胞,在外周区可见CD3+的T细胞和少量CD20+的B细胞,证实了免疫细胞的参与。
- IgG, IgM, RF:在中心的坏死区中常常可以检测到免疫球蛋白和类风湿因子的沉积,直接证明了免疫复合物在结节形成中的核心作用。
形成机制
类风湿小结的形成是一个复杂的免疫介导过程:
(图片来源网络,侵删)
- 免疫复合物形成:在关节滑膜或其他部位,抗原(如瓜化蛋白、免疫球蛋白)与自身抗体(尤其是类风湿因子RF和抗瓜化蛋白抗体ACPA)结合,形成免疫复合物。
- 血管炎与渗出:这些免疫复合物沉积在小血管壁上,引发血管炎,导致血管通透性增加,血浆中的纤维蛋白原等成分渗出到组织中。
- 坏死中心形成:沉积的免疫复合物激活补体系统,吸引并激活中性粒细胞,中性粒细胞释放蛋白酶和活性氧,导致局部组织坏死,并与渗出的纤维蛋白原混合,形成中心的“纤维素样坏死”。
- 肉芽肿形成:坏死物质作为强烈的“异物”,吸引巨噬细胞聚集,巨噬细胞在坏死区边缘被激活,转变为上皮样细胞,并呈栅栏状排列,形成肉芽肿结构。
- 慢性化与纤维化:持续的炎症刺激导致外周的成纤维细胞增生,并产生胶原纤维,最终将整个结节包裹起来,形成纤维性包囊。
临床意义
- 诊断价值:类风湿小结是类风湿关节炎的特征性表现之一,在临床诊断标准(如ACR/EULAR标准)中,它的存在是重要的诊断依据。
- 疾病活动度的标志:结节的出现通常与血清类风湿因子滴度高、疾病活动度高以及关节外表现相关。
- 治疗反应:有效的抗风湿治疗(如改善病情抗风湿药DMARDs,尤其是甲氨蝶呤)通常可以使类风湿结节缩小甚至消失。
| 结构层 | 主要成分 | 病理特征 |
|---|---|---|
| 中心区 | 纤维蛋白、免疫复合物、核碎片 | 纤维素样坏死,无结构,嗜伊红性 |
| 中间区 | 巨噬细胞/上皮样细胞、成纤维细胞 | 栅栏状排列,肉芽肿性炎症 |
| 外周区 | 淋巴细胞、浆细胞 | 慢性炎症细胞浸润 |
| 最外层 | 胶原纤维 | 纤维组织包囊,将结节与周围组织隔离 |
类风湿小结是一个由免疫复合物驱动的、具有明确分层结构的局灶性坏死性肉芽肿,它直观地展现了类风湿关节炎作为一种系统性自身免疫疾病的本质。
(图片来源网络,侵删)




